近年来,免疫检查点抑制剂(Immune checkpoint inhibitor,ICI)的使用,例如抗CTLA-4 以及抗PD-1/PD-L1单抗,给肿瘤治疗带来了革命性的变化【1】。但是,在接受ICI治疗之后,只有一小部分病人能够获得持续的疗效,最近的几个大型临床三期实验也都报道了阴性结果【2, 3】,迫使研究人员去寻找对ICI治疗反应良好的预测标记。早期的研究表明,PD-L1免疫组化水平,T细胞浸润程度,T细胞受体的克隆特征,基因表达谱系,以及外周血中得一些标记都可能与ICI的临床治疗效果相关【4】。在一些黑色素瘤和非小细胞肺癌小型队列研究中,研究人员观察到高的肿瘤突变荷载(tumor mutational burden,TMB)与较好的ICI治疗疗效相关【5, 6】。但是对于其他更多类型的肿瘤,以及在更广泛的病人中,TMB是否能预测ICI治疗效果还有待证明。
近日,来自Memorial Sloan Kettering Cancer Center (MSK)的Timothy Chan,David Solit,Luc Morris及同事在Nature Genetics上发表题为Tumor mutational load predicts survival after immunotherapy across multiple cancer types的文章,通过大样本的测序分析,表明了肿瘤突变荷载(TMB)可能是一个可用于预测不同类型肿瘤患者对免疫检查点抑制剂免疫疗法反应的有用指标。
在Memorial Sloan Kettering Cancer Center,Integrated Mutation Profiling of Actionable Cancer Targets (MSK-IMPACT) 测序检测【7】作为对患者临床治疗的一部分而被批准进行,研究团队从MSK-IMPACT中获得肿瘤患者的肿瘤突变荷载(TMB)水平。然后他们分析TMB和ICI治疗后患者生存率的关系,这一队列包括1662名肿瘤患者,其中包含了多种不同类型的肿瘤。由于来源不同组织的肿瘤,其突变荷载也大不相同,所以关于TMB亚群的分类,研究人员依据肿瘤的组织类型不同而不同。从整个队列来看,结果如下图,较高的突变荷载的确与较好的总体生存相关。
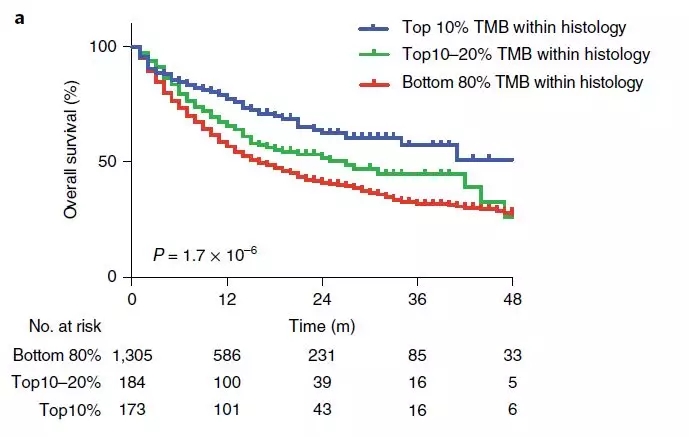
图1 不同TMB水平肿瘤患者的Kaplan–Meier生存曲线。
他们也对每一种类型的肿瘤单独做了TMB和总体生存率的关系分析,也得到了相似结果。TMB分布程度因肿瘤组织类型不同而不同,同样地对于不同组织类型的肿瘤,并没有一个固定的数值去定义为ICI治疗反应良好的“高TMB”值。研究团队同时也分析了另一包含5371名未接受ICI治疗的肿瘤患者队列, 他们发现在这些病人中,较高的TMB和较好的总体生存之间并不存在相关关系,再次表明TMB是作为ICI治疗效果的一个预测标记。
总之,本研究表明肿瘤突变荷载(TMB)或可是一个预测不同类型肿瘤患者对免疫检查点抑制剂(ICI)免疫疗法反应的有用指标。
原文链接:https://www.nature.com/articles/s41588-018-0312-8