病毒感染可以引起多种疾病,严重威胁人类健康。但机体也并非坐以待毙,而是进化出多种方式感知病毒的感染并通过激活自身的免疫系统清除体内的病毒。病毒的感染诱导干扰素产生,而干扰素上调多种干扰素刺激基因(ISGs)的表达。根据已有报道,ISGs在HIV-1 病毒复制期的多个步骤以不同机制抑制病毒【1】。
由于体积的限制,病毒的基因组通常比较小,所携带的遗传信息比较少。病毒在复制过程中,会利用一些特殊的机制扩展其所携带遗传信息的利用率,其中一种常用的机制是称为程序性移码的蛋白质合成重编码机制。病毒RNA上含有程序性移码信号,核糖体翻译蛋白过程中遇到此信号时会发生停顿,其中大部分核糖体以原来的读码框翻译,但有一小部分核糖体在RNA上发生滑动,以新的读码框继续翻译【2】。结果是病毒利用一条RNA为模板翻译产生两种蛋白,其N-端序列相同,但C-端序列不同。如果核糖体后退1个核苷酸,则称为-1位程序性移码(Programmed -1 Ribosomal Frameshifting,简称-1PRF)。HIV病毒利用-1位程序性移码翻译结构蛋白Gag和包含复制酶的Gag-Pol蛋白【3, 4】,是病毒复制过程中必须的一个重要步骤。-1位核糖体移码效率决定病毒蛋白Gag/Gag-pol比例,比例失衡会严重影响病毒粒子的复制 【5, 6】。既然-1PRF对HIV-1如此重要,很可能是细胞抗病毒的一个重要靶点,但是人们对宿主因子如何通过调控程序性移码而达到抗病毒目的却知之甚少。
1月24日,中国科学院生物物理所的高光侠团队在Cell杂志发表了题为Regulation of HIV-1 Gag-Pol expression by Shiftless, an inhibitor of programmed -1 ribosomal frameshifting的研究长文,该研究鉴定到一个新的宿主抗病毒因子(命名为Shiftless,简称SFL),抑制病毒蛋白翻译过程中的程序性-1位核糖体移码;并进一步揭示了SFL作用的分子机制。
为了筛选抑制-1PRF效率的宿主因子,高光侠团队首先确证了干扰素抑制HIV-1 Gag-pol蛋白/Gag 蛋白的比例,由此推断干扰素通过上调特定ISG抑制-1PRF效率。 随后以-1PRF报告基因为筛选模型对99个ISGs进行筛选,发现其中一个 (命名为Shiftless)的表达产物特异性抑制-1PRF。进一研究发现,SFL表达通过抑制HIV-1 的-1PRF 效率,直接导致Gag-pol蛋白表达水平的降低。
前面讲到,HIV-1 的Gag-pol蛋白是病毒复制必须蛋白之一,Gag-pol可加工成多种结构蛋白和HIV-1复制必须的酶活性蛋白,对病毒粒子的加工成熟及感染力至关重要。实验结果证实,SFL导致的Gag-pol水平降低影响了病毒粒子的加工成熟,进而抑制了HIV-1病毒在细胞中的复制。这些结果表明,SFL是一个新的抗HIV-1蛋白,通过影响-1PRF效率而抑制病毒复制。
程序性移码机制最早在病毒中发现,但后来发现该机制在所有生物中均存在【7】,而且除了用于翻译重编码,还可以调控mRNA的稳定性 ADDIN EN.CITE 【8】。研究者分析了多种病毒及细胞内mRNA中-1PRF对SFL的敏感性,发现SFL对多种病毒的-1PRF都有抑制,并影响这些病毒的生活周期;细胞内已知的几个发生-1PRF的基因对SFL 也有响应。上述结果表明SFL是一个广谱的-1PRF抑制剂。
研究人员对SFL的作用机制也进行了探索。-1PRF的发生依赖于mRNA上的-1PRF 信号,以及翻译中的核糖体【7, 9】。通过一系列生化实验发现,SFL直接结合-1PRF信号序列,同时结合处于-1位移码状态的核糖体。这些相互作用是SFL抑制-1PRF的关键。
研究者还观察到SFL导致一种未成熟翻译终止产物(PMT,premature translation termination)的产生,并对PMT产物进行了质谱分析,发现PMT终止在-1PRF信号位置。如果敲低细胞内源eRF3-eRF1复合体(细胞内参与蛋白翻译终止的的一种蛋白复合体),PMT的产物会相应减少。由此,研究者推断SFL使-1位移码的核糖体停滞在移码信号位置,并招募eRF3-eRF1复合体把该核糖体从mRNA上解离下来,导致PMT的产生。
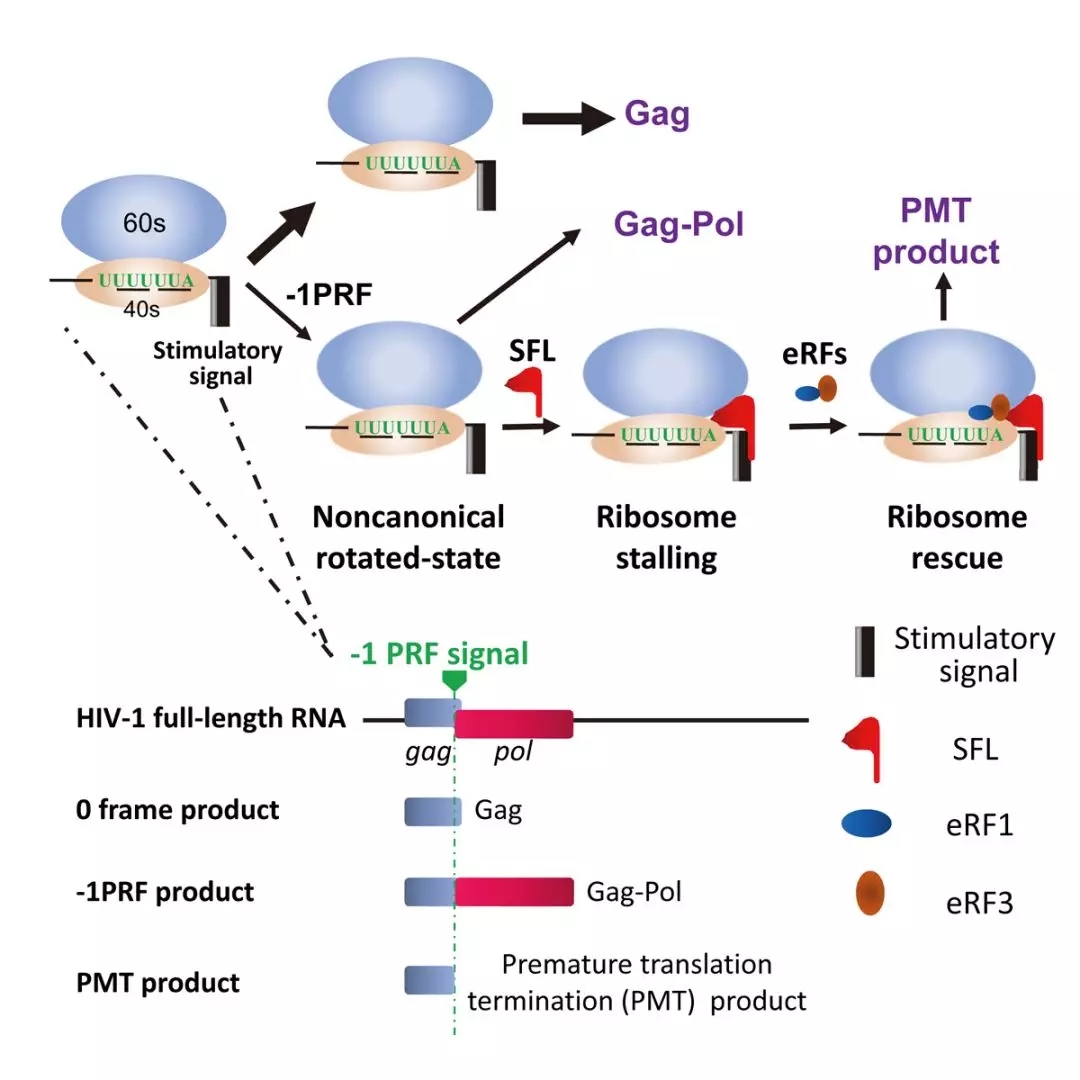
综合上述实验结果及相关领域内知识,研究者提供了SFL可能的作用机制模式图(下图):HIV-1全长RNA 用于Gag蛋白的翻译。核糖体翻译到临近Gag C端位置时,遇到mRNA上的-1PRF信号,一部分核糖体发生-1位移码产生Gag-pol。-1位移码状态的核糖体,其大小亚基构象改变,处于一种停滞时间延长的非经典旋转状态,暴露出适合SFL结合的表面。SFL同时与-1位移码序列及核糖体结合,阻碍了核糖体构象复位。这种处于翻译停顿状态的核糖体需要被及时清除,以保证细胞功能正常运行。这时eRF1-eRF3复合体被招募到停滞的核糖体部位,解离核糖体,产生PMT产物是核糖体拯救过程的副产物。
程序性移码是一种蛋白质合成重编码机制,由一条RNA通过两条路径合成2个不同的蛋白。HIV病毒采用该机制表达其复制所必需的Gag和Gag-pol蛋白。高光侠团队报道宿主因子SFL抑制程序性移码,从而抑制病毒复制。本图展示了这一过程:为到达山顶建立有效复制,病毒需要收集主路上的棕色蘑菇(Gag蛋白)和支路上的紫色蘑菇(Gag-pol蛋白)。熊猫(SFL)堵在支路上,阻碍病毒建立有效复制。
该项研究成果对多个相关领域研究都有重要意义:
1)病毒与宿主相互作用:HIV-1复制多个步骤都受宿主限制性因子的作用,-1PRF作为HIV-1周期的一个重要步骤和潜在靶点,一直未见调控机制报道。该项研究弥补了这一空白。深入研究病毒与宿主相互作用,一方面有利于深入了解病毒的复制和致病机制,另一方面还能为临床诊疗和新药研发提供新的靶点和理论基础。
2)病毒学研究从来不局限于病毒本身。作为最小的可复制的生物体,病毒也是一种模式生物,被广泛用来探索普遍意义生物学规律。程序性移码机制最早在病毒中发现,但后来发现该机制在所有生物中均存在,而且除了用于翻译重编码,还可以调控mRNA的稳定性。在高等生物mRNA中,生物信息学预测,含程序性移码信号的mRNA可能多达2000个,但目前为止经过验证的只有极少数几个。程序性移码是如何进行的?是如何受调控的?这些重要问题都有待解答。作为第一个被发现的-1位程序性移码调控因子,SFL的研究将为进一步深入研究-1位程序性移码的作用机理提供了有效的工具。
原文链接:https://www.cell.com/cell/fulltext/S0092-8674(18)31644-1