成年人的心脏几乎不具备自愈和再生能力,一旦受损就难以恢复到之前的状态。这种不可修复的损伤是因为心脏中的心肌细胞几乎丧失分裂的能力造成的。哺乳动物心脏是一种高性能器官,作为身体血液循环的中心,它持续产生的强压将血液泵至身体各个部分。为了维持心脏的高性能,心肌细胞之间永远非常紧密地连接在一起,形成了一个所谓的电荷体,为其收缩的所需电传导提供了必不可少的可控性。所以由分裂产生的心肌细胞很可能会破坏这一个生理过程而导致心脏不同步。因此,与其他具有高再生能力的器官相比,在心脏中并没有可分裂和再生的干细胞。这导致,当部分心肌受损时,比如心脏病发作,心脏并不具备自我修复的能力,从而影响了心脏的功能。
由德国马克思普朗克心肺研究所(Max Planck Institute for Heart and Lung Research, Bad Nauheim)科学家牵头组建的国际性研究小组在最近的研究中发现,通过控制重编程因子对心肌的改变而促进其在体内的增殖,能够实现小鼠损伤心脏的再生。在此过程中,对心肌细胞重编程的强度和持续时间的控制最为重要,太弱不能帮助心脏再生,太强则导致肿瘤的形成。这项研究成果于近日发表于Science杂志,题为:Reversible reprogramming of cardiomyocytes to a fetal state drives heart regeneration in mice。
哺乳动物的心肌细胞在其胚胎和初生阶段具有一定的分裂能力,但是当成其年后,心肌细胞的分裂变得极为罕见。从这些有限的分裂中发现,它通常需要激活一些只存在于心脏早期发育中的基因的表达。换句话说,成年的心肌细胞需要在某种条件下去分化或退回到类似发育的早期阶段,从而获取在这种状态下的分裂能力。
马克斯普朗克心肺研究所"心脏发育和重塑"部门的科学家们在小鼠身上研究了否可以通过一种对心肌细胞采用短暂的强制重编程的方式来促进受损心脏的再生。这项研究由Johnny Kim和Thomas Braun 共同领导(第一作者陈焱埔)。他们使用四种干细胞因子共同作用于心肌细胞来实现心肌细胞的去分化,从而刺激它进入细胞周期。为此,该课题组构建一种转基因小鼠,它的心肌细胞能特异性的开启和关闭Oct4、Sox2、KLF4和c-Myc(缩写为OSKM)的表达。OSKM的表达具有诱导体细胞重新编程和产生诱导性多能干细胞(iPSC)的能力。iPSC类似于胚胎干细胞,它们能分化成人身体所有细胞类型,其发现者山中伸弥为此获得了2012年的诺贝尔生理学或医学奖。
利用构建的转基因小鼠,科学家在分离的心肌细胞中成功开启了OSKM的表达。在这些因子的作用下,他们观察到心肌细胞的去分化,心肌细胞开始分裂。此后,研究人员也研究了OSKM在小鼠体内心肌中的开启和关闭对心脏的影响。连续六天表达OSKM,他们发现心肌中基因组表达发生了变化,最明显的是参与细胞分裂和代谢调控相关的基因。OSKM表达关闭后,这些基因几乎恢复到原来的水平;在整个过程中心脏的功能并没有受到影响。然而,OSKM在体内心肌细胞中过长时间的表达会导致心脏出现不可逆的变化,其中包括其功能的损伤。当体内心肌细胞的无休止地表达OSKM后,心肌细胞会去持续去分化以致失去了原有的特性,甚至导致心脏肿瘤的形成。
这些初步的研究证明,通过对OSKM表达的开关使控制心肌细胞的去分化和分裂成为了可能,为此科学家们也研究了是否能利用这一过程实现心脏损伤的修复。在小鼠心肌梗塞模型中,OSKM在心肌细胞中的可控表达能实现心脏的再生;相比与对照组,小鼠经过短暂OSKM表达后心脏损伤的疤痕有明显的减小。通过对心肌梗死模型前后心脏功能的检测,损伤手术前和手术中有短暂OSKM表达的小鼠的心脏功能也得到了明显的改善。
总结来说,这项研究表明,当不可分裂的细胞被赋予分裂的能力后,弱再生能力器官的功能得到了恢复。然而,研究者也观察到了心脏肿瘤的产生,所以应用到临床还有很长一段路要走。这项研究也进一步揭示了癌症与再生之间的天然联系:细胞分裂多的器官具有更高的再生能力,也具有较高产生癌症的可能,而像心脏这样再生能力差的器官却显示出较低的癌症风险。但是,如果增加心脏再生能力,其患癌的风险也会提升。不幸的是,生活中没有什么是“免费”的。
这项研究探索了在体心肌细胞重编程,实现了小鼠成体心肌细胞的分裂和损伤心脏的再生。为此,Science发表了专门评述:Reversing aging for heart repair。OSKM疗法在人体的应用尚有很长的路,表达量的严格控制是限制心肌细胞无序扩增的关键。可开发RNA或者小分子药物来操控OSKM的表达。
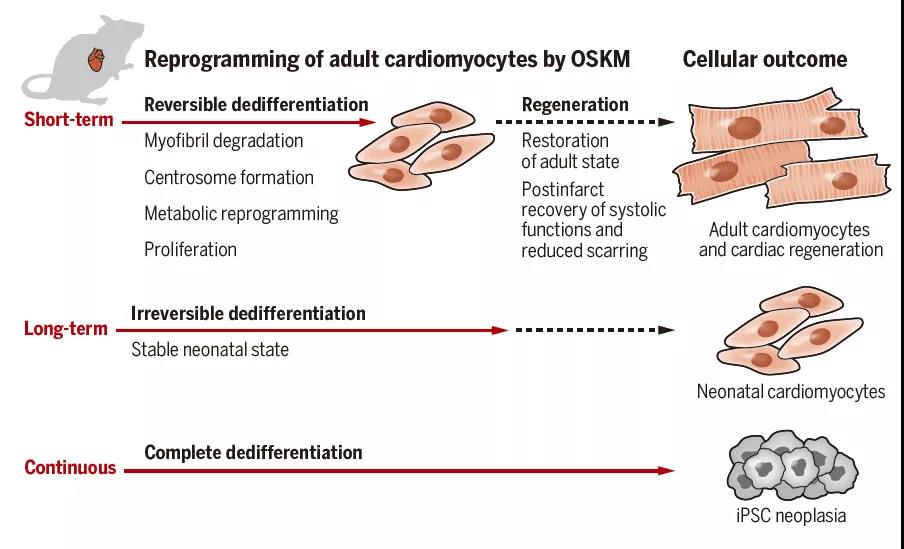
心脏再生:调控因子(OSKM: = Oct4, Sox2, Klf4, c-Myc)的在成年小鼠心肌细胞中的短暂表达使心肌细胞发生重编程,从而使它退回至类似早期发育阶段的心肌细胞,从而暂时恢复了分裂的能力。分裂的心肌细胞填补了心脏病发作造成的缺口,避免了疤痕的产生,实现了损伤心脏的再生。
原文链接:
https://www.science.org/doi/10.1126/science.abg5159