近日,我院在非编码RNA及氧化修饰研究领域取得的研究成果发表于 Molecular Cell杂志和Nature Communications杂志。
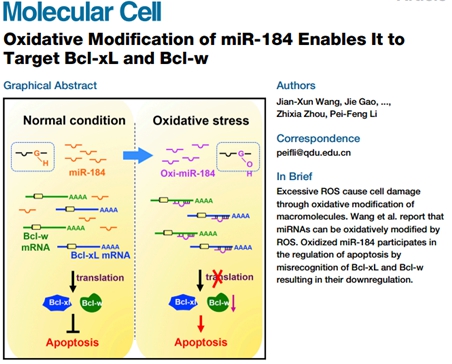
过量的活性氧(reactive oxygen species, ROS)能够通过氧化修饰生物大分子使其功能异常,从而引起细胞损伤效应。而这样的氧化修饰与癌症、衰老、神经退行性疾病以及心血管疾病等相关。在Molecular Cell文章中,我们研究证实经氧化修饰后的miR-184会发生错配结合于并非其天然靶标的Bcl-xL和Bcl-w的3′ 非翻译区,调控基因的表达。同样,我们分别在细胞和动物水平上证实了氧化miR-184与Bcl-xL和Bcl-w的这种错配参与启动细胞的凋亡。以上的研究结果揭示了ROS通过氧化修饰miRNA来参与调控心肌细胞凋亡的模式。该研究发表在Molecular Cell上,作者有王建勋教授等。
在Nature Communications文章中,研究发现了一种lncRNA可以调节心肌细胞的自噬,并将新发现的lncRNA命名为自噬促进因子(autophagy promoting factor,APF)。研究结果显示miR-188-3p可通过作用于自噬相关基因ATG7来抑制自噬引起的心肌细胞死亡或心肌梗死。 APF可以靶向miR-188-3p来调节ATG7的水平进而起到调节心肌细胞自噬和心肌梗死的作用。该研究揭示了由心脏中的APF、miR-188-3p和ATG7组成的新的调节心肌细胞自噬程序的信号通路。该通路中的相关因子可以为开发针对心肌梗死和心力衰竭的新治疗策略提供潜在的作用靶点和诊断工具。该研究发表在Nature Communications上,作者有王昆教授等。

原文链接:
Oxidative Modification of miR-184 Enables It to Target Bcl-xL and Bcl-w. Molecular Cell. DOI: http://dx.doi.org/10.1016/j.molcel.2015.05.003
APF lncRNA regulates autophagy and myocardial infarction by targeting miR-188-3p. Nature Communications 6, Article number: 6779 doi:10.1038/ncomms7779