近年来最重要的科学进步包括利用一种快速的负担得起的CRISPR技术发现和开发对生物进行基因改造的新方法。如今,在一项新的研究中,来自美国德克萨斯大学奥斯汀分校的研究人员表示他们对这种技术进行简单地改进,这将导致它更准确地和更安全地进行基因编辑,从而为足以安全地在人体中进行基因编辑打开大门。
这些研究人员发现确凿的证据表明作为当前用于CRISPR基因编辑的最受欢迎的酶,也是第一个被发现的CRISPR蛋白,Cas9在基因编辑效率和精确度上低于一种较少使用的被称作Cas12a(之前被称作Cpf1)的CRISPR蛋白。相关研究结果于2018年8月2日在线发表在Molecular Cell期刊上,论文标题为“Kinetic Basis for DNA Target Specificity of CRISPR-Cas12a”。
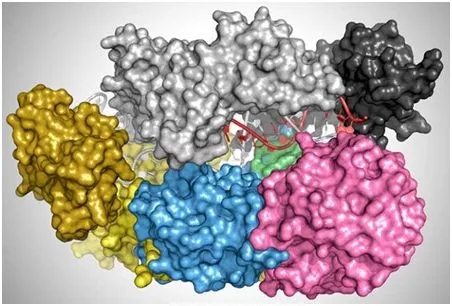
鉴于Cas9更有可能在植物或动物基因组的错误位点上进行编辑,从而破坏健康的功能,这些研究人员认为切换到Cas12a将导致更安全的更有效的基因编辑。
论文共同作者、德克萨斯大学奥斯汀分校分子生物科学助理教授Ilya Finkelstein说,“总体目标就是发现大自然给我们提供的最好的酶,然后让它变得更好,而不是采用由于历史偶然事件而被发现的首个酶。”
科学家们已利用CRISPR---细菌用来抵御病毒的一种天然机制---更多地了解人类基因,对植物和动物进行基因改造,并取得受到科学小说启发的进步,比如培育出含有抗肥胖小鼠基因的猪,从而获得更瘦的熏肉。许多人期待利用CRISPR能够开发出新的更好的人类疾病疗法和具有更高产量或抵抗干旱和害虫的作物。
但是在自然界中发现的CRISPR系统有时会靶向基因组中的错误位点,因此当将它用于人类中时,这可能会带来灾难性的后果,比如它未能校正导致遗传疾病的基因突变,而是将健康细胞转变为癌细胞。
之前的一些研究已提示着Cas12a比Cas9更加挑剔,但是在此之前这一切尚无定论。这些研究人员说,这项最新研究最终证实Cas12a是一种比Cas9更精确的基因编辑手术刀并解释着为何会如此。
在Rick Russell教授和研究生Isabel Strohkendl的领导下,这些研究人员发现Cas12a更加挑剔,这是因为它像魔术贴(Velcro)那样结合到基因组靶位点上,而Cas9更像是强力胶(super glue)那样结合到它的靶位点上。对这两种酶而言,它们中的每一种酶都携带着一小段RNA(即向导RNA, gRNA),其中gRNA与靶DNA片段相匹配。当接触到某种DNA片段时,每一种酶都开始尝试着通过形成碱基对来结合到这种DNA片段上---从它的一端开始并沿着它前进,并进行测试以便观察DNA上的每个碱基与gRNA的匹配程度。
对Cas9而言,每个碱基对紧紧地结合在一起,就像少量的强力胶一样。如果gRNA和DNA的前几个碱基匹配良好,那么Cas9已与DNA紧密地结合在一起。换句话说,Cas9会关注基因组靶标中的前七个或八个碱基,但随着这个匹配过程继续进行,它就不那么注意后面碱基的匹配性,这意味着它很容易忽略这个匹配过程后面发生的不匹配,这会导致它在基因组的错误位点上进行编辑。
对Cas12a而言,它更像是一个魔术贴扣带。在沿着DNA前进的每个位点上,它与DNA位点之间的结合相对较弱。为了让gRNA和DNA足够长时间地结合在一起而进行基因编辑,这就需要这两者在整个过程中都存在很好的匹配。这使得它更可能仅对基因组中的预期部分进行编辑。
Russell说,“这使得碱基对形成过程是更加可逆的。换句话说,Cas12a能够更好地检查每个碱基配对,随后才移动到下一个碱基。在移动7到8个碱基后,Cas9停止检查,然而Cas12a继续检查大约18个碱基。”
这些研究人员表示Cas12a仍然不完美,但是这项研究还提出了对Cas12a进行进一步改进的方法,也许有一天会实现创建“精确手术刀(precision scalpel)”的梦想,这本质上是一种防错的基因编辑工具。
Finkelstein说,“总的来说,Cas12a更好,但是令人吃惊的是,在有些地方,Cas12a仍然对gRNA和基因组靶标之间的错误配对视而不见。因此,我们所要做的是为进一步改进Cas12a提供明确的前进道路。”
参考资料:
Isabel Strohkendl, Fatema A.Saifuddin, James R.Rybarski et al. Kinetic Basis for DNA Target Specificity of CRISPR-Cas12a. Molecular Cell, Published Online: 02 August 2018, doi:10.1016/j.molcel.2018.06.043.