昼夜节律是一种内源性的计时系统(生物钟),几乎所有的动物都遵循与日出日落有关的昼夜节律。这些受自然光影响的节律,控制着机体一系列生物过程,包括激素分泌、代谢循环和对病原体的免疫保护,也诱导了我们充满节律的自然行为,如吃饭和睡觉。一旦逆其道而行之,身体就会变得脆弱。此前,发表在《PLOS Computational Biology》上的一项研究阐明了不规律的作息时间与免疫系统受损有关,进而影响了身体抵抗感染的能力。近日,发表在 Cell 上的一项新研究中,来自美国德克萨斯大学西南医学中心(UTSW)的研究团队同样告诉我们,免疫系统并不是“时刻准备着”,它也被昼夜节律所调控。

该研究表明,身体抵抗感染的能力会在一天中起起落落,在应该睡觉的时间最弱。所以说,你要熬夜,你要吃夜宵,但你的免疫系统不会陪着你一起,而在这种情况下,你更容易受到感染。
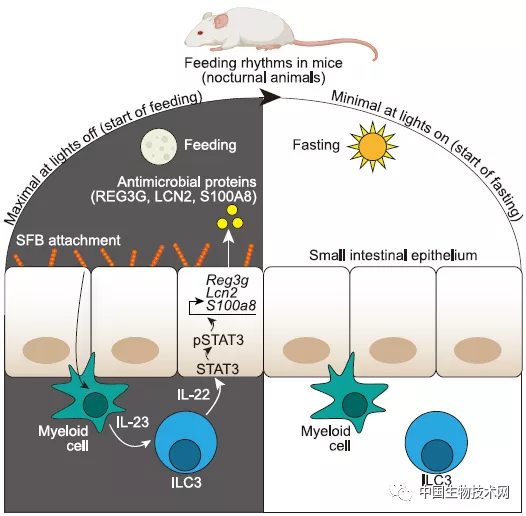
生物钟是一个转录因子网络,几乎存在于所有的组织中,并通过来自大脑核心时钟的神经元和激素信号与环境光的周期同步,在一个约24小时的周期内驱动有节律的基因表达,从而预测和应对环境的变化。已知熬夜或慢性睡眠中断与人免疫力减弱有关。例如,与白天工作的人相比,上夜班的人对细菌和病毒感染的易感性更高。然而,对这一问题的致病机制还未被阐明。在哺乳动物中,进食行为会使自己暴露于与食物和环境相关的微生物中。为了防止感染,肠上皮细胞会产生先天免疫效应因子,包括分泌大量的抗菌蛋白(AMP),但产生AMP的代价是昂贵的,因为需要耗费掉大量能量。这也就意味着,肠道先天免疫存在高峰和低谷。研究人员推测肠道内的抗菌免疫力同样会遵循昼夜节律变化。为此,他们研究了在小鼠肠道中产生的对抗食源性疾病的天然抗菌蛋白的表达节律。他们通过小鼠实验发现肠道菌群和生物钟协同产生了肠道先天免疫的昼夜节律。具体而言,小鼠的进食行为促进了肠道分段丝状菌(SFB)节律性地附着于肠上皮,并驱动上皮细胞信号传导和转录激活因子3(STAT3)的表达和激活振荡,从而产生了一种被称为再生胰岛衍生蛋白3γ(REG3G)的抗菌分子在夜间的含量更高(此时为夜行性动物的活跃状态);而在白天睡眠时含量较少。但在无菌小鼠体内,无论白天还是晚上,REG3G基本上都不存在。
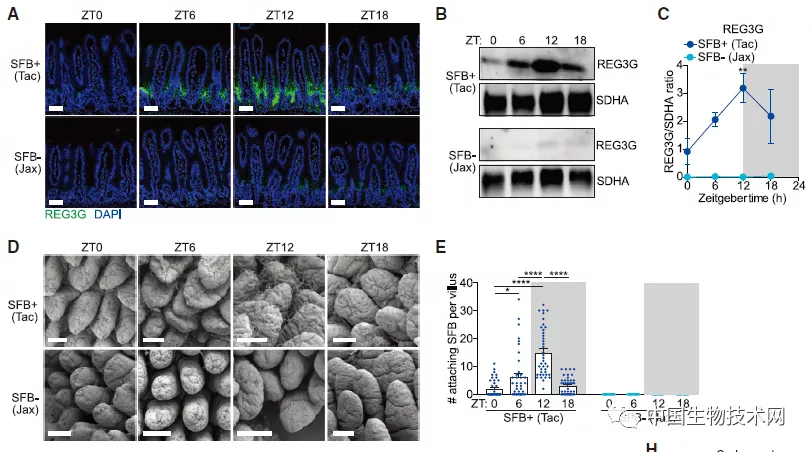
分段丝状细菌(SFB)通常存在于啮齿动物、非人灵长类动物以及人体肠道内。具有附着于肠道内壁并改变其宿主基因活性的独特能力。通过进一步的实验表明,这些细菌在动物进食期间附着在其肠内壁上,也许是为了摄取营养。研究人员发现,当它们附着时,REG3G在肠道中的产量急剧上升。昼夜节律对小鼠抵抗感染的能力产生了重大影响。当研究人员用细菌感染正常小鼠时,他们发现,在白天(睡眠时间),这些小鼠的细菌负荷和死亡率更高。然而,对于体内不能产生REG3G的小鼠而言,无论什么时间被感染,其细菌负荷和死亡率都同样高。研究人员表示,进食行为的改变或许是一个致病因素。如果进一步的研究表明这种现象也发生在人类身上,那么科学家可以利用这种机制,制定更有效的定时治疗干预策略,包括什么时间接种疫苗更有效。研究通讯作者、UTSW免疫学系副教授Lora Hooper说:“这项研究结果让我在半夜起来准备到冰箱里找些吃的的时候要三思了,因为那正是我肠道防御能力最弱的时候,吃富含细菌的食物可能是危险的。”
论文链接:https://doi.org/10.1016/j.cell.2021.07.001